如今,癌症的精准医疗已经不是什么神秘又高冷的名词了,在消费级基因检测的推广和各种科普下,不知道点什么“液体活检”“基因测序”“循环肿瘤DNA(ctDNA)”之类的名词可真是有点落伍了。
在科研领域飞速发展的同时,临床医生们也与时俱进,抽血做个基于ctDNA的液体活检,一方面可以又快又准确地帮助医生进行早期诊断,另一方面,对于已经确诊了的患者,还可以制定个性化的治疗方案,隔一段时间检测一次又可以动态地监测肿瘤的发展情况,及时对治疗方案做出调整。相比于传统的组织活检,通过外周血液的液体活检可以避过肿瘤异质性、穿刺导致癌细胞转移等诸多问题。
可是,在当下液体活检风头正盛的时候,约翰霍普金斯大学医学院的两位研究人员却在《JAMA Oncology》杂志上发表研究指出,不同机构进行的检测得到的结果差异非常大,两家权威机构同时检测的40名患者样本中,除去6例检测结果被认为无效的外,其余34例中测序结果完全一致的只有12例[1]!
来自约翰霍普金斯大学医学院的两位研究人员,Gonzalo Torga(左)和Kenneth J. Pienta(右)
需要注意的是,两家机构检测的基因和位点都有一些差异,因此研究人员只比较了两家公司的检测中共有的、重合的位点。基于这一结果,他们认为这一结果值得科学家们深思,究竟该怎样改善现有的方法才能更好地帮助到患者。
在这次的研究中,“接受考验”的两家机构分别是Guardant Health和Personal Genome Diagnostics,两家的检测产品会分别对患者血液样本中的73个基因和64个基因的部分编码序列进行测序。
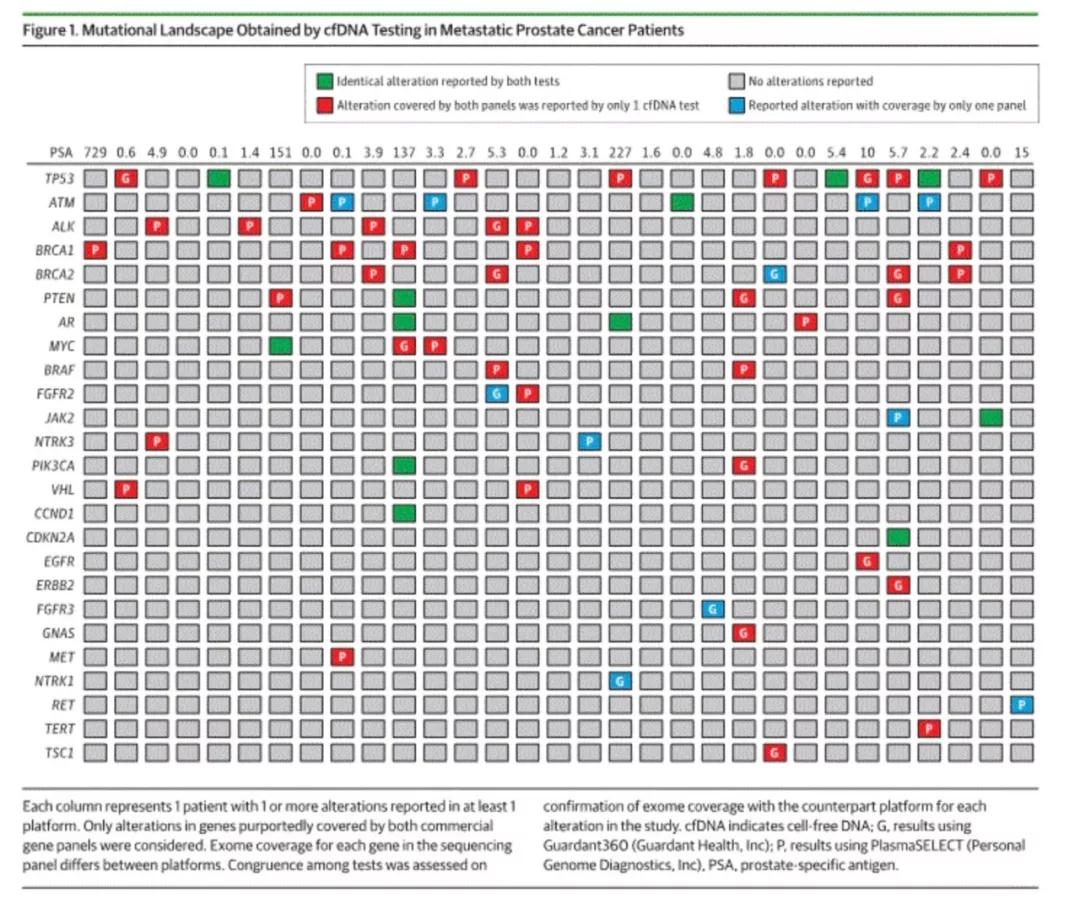
绿:两家检测都发现的重合的突变位点,灰:没有检测到突变的位点,红:两家重合的检测位点中只被其中一家检测到的,蓝:其中一家特有的检测位点被检测到突变的;P代表Personal Genome Diagnostics,G代表Guardant Health
Personal Genome Diagnostics的创始人是约翰霍普金斯大学Kimmel癌症中心的肿瘤学教授Luis Diaz,在癌症领域有超过25年的研究经验[2],在2010年成立了Personal Genome Diagnostics。而Guardant Health可能更加为业内人士所熟悉,在成立的4年中,他们共获得了5.5亿美元的投资,还在2014年被达沃斯评为了“24家正在改变未来的公司”之一[3]。
研究人员招募了40名患转移性前列腺癌的患者,抽取了血样后,分成两份分别送到两家的实验室进行测序。在这40例样本中有6例因为某些原因检测结果被认定无效,剩下的34例中,有12例(35%)检测报告给出的结果相同,其中有3例突变谱完全一致,其余9例均没有检测到突变。剩下的22名患者就没这么“好的运气”了,他们中有6例检测到的突变有重合,但是又不完全相同,还有16例检测到的突变完全不重合。
40名患者的检测结果,16例(红)为两家检测到的突变完全不重合,6例(橙)为部分重合但不完全相同,3例(绿)为突变谱完全重合,9例(灰)为经两家检测均没有发现突变,6例(蓝)为检测结果无效
这个结果让研究人员非常惊讶,两家公司都是业内顶尖的,他们的实验室也都获得了临床检验改进修正计划(Clinical Laboratory Improvement Amendments,CLIA)的认证,CLIA认证意味着实验室中临床试验结果的准确性、可靠性和时效性都得到了FDA和CDC等的认可,并且他们也都拥有美国病理学会的CAP(College of American Pathologists)认证,“两证俱全”。
研究人员的本意也是希望为患者提供最好的选择,所以才找了两家公司提交样本,进行比较,但是这个结果让他们也很意外[4]。这也和今年早些时候同样发表在《JAMA Oncology》上的另一篇文章[5]“不谋而合”。
这项研究由华盛顿大学医学院的研究人员领导,他们招募了9名癌症患者(5名为乳腺癌,其余4名分别为胰腺癌、胸腺癌、肺癌和唾液腺癌),同样选择了两家液体活检公司对患者的血液样本进行了检测。其中一家是和这次一样的Guardant Health,另一家是Foundation Medicine,同样也是大名鼎鼎,曾为乔布斯老爷子进行过测序,创始人是人类基因组计划的领导者之一,他们的检测会包括315个癌症相关基因的外显子以及28个重排基因的内含子。
然而,2份测序结果也有不小的差异。其中胸腺癌患者在两家都没有检测到突变,剩下的8名患者中共检测到了45个突变,其中只有10个(22%)是重合的,而且8名患者中有2名检测到的突变完全不同。
这是不是说明这些检测“不靠谱”呢?但是和新研究同期刊发的另一篇文章似乎又给予了否定的回答。在研究中,研究人员使用FDA批准的伴随诊断(FDA-CD)和实验室自主开发的检测(LDT)分别对6897例样本的BRAF、EGFR和KRAS基因的突变情况进行了检测[6]。前面我们提到的几家公司的测试就属于LDT的范畴。与需要FDA进行认证,可以商用的FDA-CD相比,LDT是由各实验室自己进行研发和验证的,技术和检测只能在自己的实验室内使用,不需要FDA认证。
不过在这个研究中,研究人员发现,FDA-CD和LDT的检测结果重合度是非常高的,按照美国病理学会的实验室能力比对验证(Proficiency Testing,PT)给出的结果,两种检测都有超过97%的准确率。基于这个结果,研究人员认为FDA所希望的,加强对LDT的检测和监管可能是不必要的。LDT与FDA-CD的检测结果几乎完全相同,那么似乎说明,LDT在检测样本上的能力已经很合格了,但是前面两个研究中,两家LDT的结果偏差如此之大,与这个研究得到的结果一定程度上是相悖的。
在同期杂志中,密歇根大学综合癌症中心的Daniel F. Hayes博士还为此撰写了一篇评论文章[7],他认为后者的研究只涉及到了3个在癌症患者中极其常见的突变基因,这个结论不能推及到更多的基因和检测上。
Daniel F. Hayes博士
回顾了两个结论相悖的新研究后,Hayes博士提出了问题:究竟哪个是“事实”?没有人知道答案。他认为约翰霍普金斯大学医学院两位研究人员的研究成果应该得到特别重视,因为“一次糟糕的肿瘤标志物检测带来的后果和糟糕的药物一样”,而现在患者所用的检测多是LDT,如果检测结果的准确性不能得到保证的话,那对于患者来说是非常可怕的一件事情。
Hayes博士表示,开发LDT的公司和实验室不能抱有“一经售出,概不负责”的态度,他将联合其他研究人员,呼吁技术的研发者去验证、改善这些被广泛用于患者的检测方法。(生物谷Bioon.com)
尊敬的 先生/女士
您已注册成功,注册信息及注意事项已发到联系人及参会人邮箱,请注意查收。如未收到,请联系大会联系人。